这个 24 岁的大脑,成为了一个暴露现有理论裂缝的窗口,让安德烈·亚拉姆短暂的生命具备了更长远的意义。

图片来源:Pixabay
撰文 菡萏
几天前,英国最年轻的痴呆症患者安德烈·亚拉姆(Andre Yarham)去世,年仅 24 岁,从起病到死亡仅仅 3 年。生前的磁共振扫描结果显示,他大脑的萎缩程度,几乎像一个 70 岁的老人。
安德烈来自英格兰诺福克,2022 年开始表现出痴呆症状。他的家人称,那时他变得越来越健忘,有时脸上还会出现茫然的表情。在他生命的最后阶段,他已经丧失了语言能力,生活无法自理,也无法控制自己的行为举止,只能终日与轮椅为伴。
安德烈·亚拉姆生前 来源:Samantha Fairbairn / SWNS
年轻的身体和早衰的大脑
痴呆症总是和衰老联系在一起。但某些类型的痴呆症可在生命早期迅速出现,并以极快的速度侵蚀大脑。额颞叶痴呆(frontotemporal dementia)正是其中之一,也是安德烈被确诊的痴呆症类型。
与首先损害记忆的阿尔茨海默病不同,额颞叶痴呆主要侵袭额叶和颞叶——这些区域位于前额后方及双耳上方,负责人格特征、行为调控和语言功能。一旦受损,患者可能出现性格突变、冲动控制障碍、语言理解或表达受限,甚至逐渐丧失沟通能力。
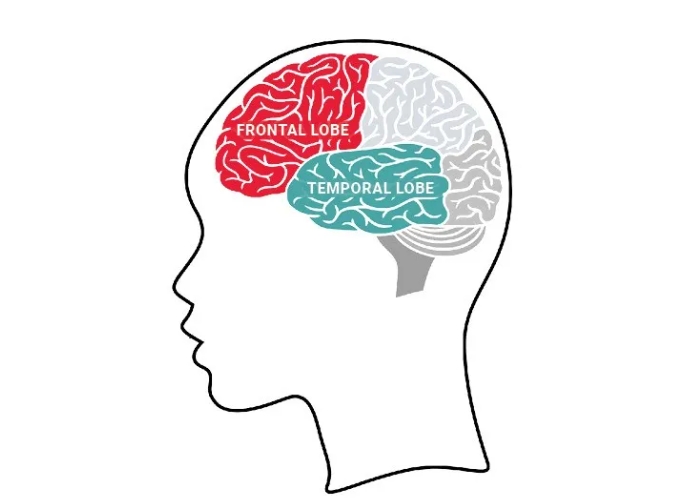
额颞叶痴呆主要侵袭额叶(红色示意)和颞叶(绿色示意)来源: Mike Mooney AFTD, CC0, https://commons.wikimedia.org/w/index.php?curid=166897324
额颞叶痴呆典型发病年龄介于 45 至 65 岁之间,然而极早发病例并非不存在。根据一项 2022 年发表的文献综述,现有记录中最年轻的额颞叶痴呆患者仅有 14 岁,此外还有至少 17 名 25 岁以下的年轻人也在学术资料里留下了他们的痕迹。安德烈也属于这一极端少见的群体。
大部分情况下,遗传因素是额颞叶痴呆的最主要病因。特定的基因突变会扰乱大脑细胞处理蛋白质的方式,导致一些毒性蛋白(如 tau 蛋白,它也被认为是阿尔茨海默病的元凶之一)无法被分解回收,反而在神经元内聚集。这阻碍了脑细胞的正常功能与存活。随着时间的推移,受影响的脑细胞会逐渐停止工作并死亡。
安德烈的家人曾向媒体透露,他的病因是一个调控 tau 蛋白的基因发生突变,导致后者异常堆积从而引起痴呆的。但他的家族内是否存在为何这一过程为何会在生命早期便开始,目前尚未完全明了。
安德烈生前的脑部磁共振成像显示,他的大脑萎缩程度对于其年龄而言异常严重。然而,这种变化并不等同于“加速衰老”。在正常老龄化过程中,大脑结构的改变通常缓慢而局限,某些区域略有变薄,但整体网络在数十年内仍保持相对稳定。
相比之下,额颞叶痴呆的核心特征是进行性的神经元丧失,主要集中于额叶或颞叶区域,纺锤体神经元的损失比例可超过 70%。随着这些关键节点迅速瓦解,支撑语言、情绪调控和决策的神经网络会在短时间内崩塌。
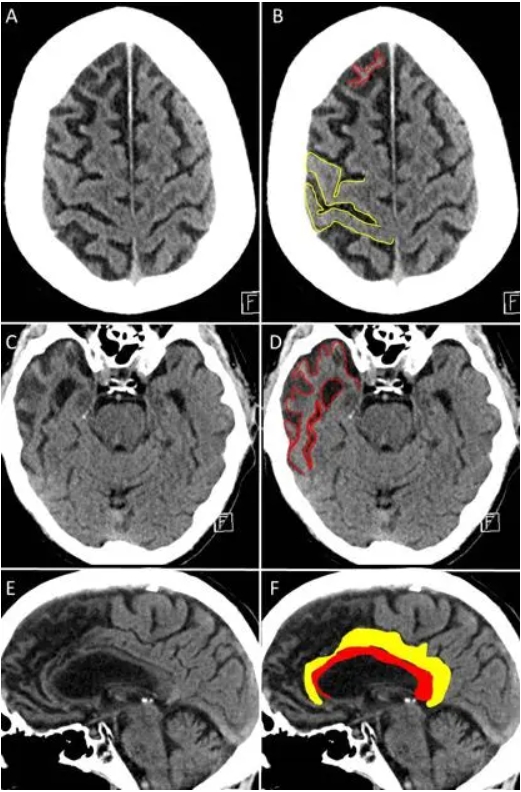
一位额颞叶痴呆患者的脑成像图,可以看到明显的额叶与颞叶萎缩。来源:radiopaedia.org
安德烈的病程清晰地体现了这一过程。他的母亲回忆,在正式确诊前,他已出现说话困难,但仍能勉强交流;而在去世前一个月,他已完全丧失语言能力,只能发出零散的声音。
照亮研究死角
安德烈去世后,家人决定将他的大脑捐献用作科研。
极早发性痴呆的大脑样本极为稀缺。脑部影像只能显示哪些区域已经受损,而只有对捐赠组织的直接分析,才能揭示细胞层面和分子层面的根本异常。研究人员可以由此确认哪些蛋白发生异常积聚、哪些类型的神经元最为脆弱,以及炎症和免疫反应如何加速病变进程。
这些信息直接关系到疾病机制的重建,也为延缓、阻止甚至预防痴呆症的治疗策略提供关键线索。
此外,与阿尔茨海默病相比,额颞叶痴呆是一种较为罕见的痴呆症,每年每 10 万人中的发病数仅为 2-3 人。这导致额颞叶痴呆在研究和临床资源分配上,长期处于阿尔茨海默病的阴影之下。许多临床试验在设计阶段即排除了年轻患者,而早发性病例在精神科与神经科之间的诊断延误也并不罕见。这种结构性忽视,使得这种疾病的自然史和机制研究进展缓慢。
像安德烈这样的极早发病例的出现,迫使研究界重新审视这种局面。它提醒人们,神经退行性疾病并不总是“晚年的问题”,而现有分类体系和研究框架可能不足以覆盖其真实复杂性。
这个 24 岁的大脑,成为了一个暴露现有理论裂缝的窗口,让安德烈·亚拉姆短暂的生命具备了更长远的意义。

生活中的安德烈·亚拉姆 来源:FitzRoyTheMaltings














































